Miksi jää on liukasta?
Kävelin juuri kotiin ja meinasin kaatua pahasti, kun kävelytie oli jään peitossa. Miksi jää onkin niin liukasta?
Tämä onkin mielenkiintoinen kysymys — ja itse asiassa yllättävän vaikea. Vaikka kyseessä on hyvin arkinen asia, vastaus tähän selkeytyi vasta 2010-luvulla?
Oho, aika yllättävää.
Totta se on. Kuten sinuakin, asia on vaivannut fyysikoita jo pitkään. Mitä sinä veikkaisit?
Käydäänpä läpi noita vaihtoehtoja yksi kerrallaan ja aloitetaan hypoteesista A. Tässä hypoteesissa oletetaan, että paineen noustessa kenkiemme alla jää sulaa vedeksi. Lasketaan ensin, että kuinka suuren voiman astuminen jäälle aiheuttaa jään pintaan. Olkoon jäällä kävelevän henkilön massa  . Tarkastellaan tilannetta, jossa henkilö on yhden jalan varassa koko painollaan. Tällöin henkilö aiheuttaa jään pintaan voiman, jonka suuruus on
. Tarkastellaan tilannetta, jossa henkilö on yhden jalan varassa koko painollaan. Tällöin henkilö aiheuttaa jään pintaan voiman, jonka suuruus on
Tämä voima aiheuttaa paineen astuttavalle pinnalle. Mikä muu tekijä kuin henkilön massa vaikuttaa paineen määrään?
Paine tosiaan on pintaan vaikuttavan voiman ja voiman vaikutuksen pinta-alan suhde. Painetta merkitään usein symbolilla  ja sen SI-yksikkö on Pascal (
ja sen SI-yksikkö on Pascal ( ). Mitä pienempi pinta, sitä suurempi paine. Esimerkiksi lumikenkien pohjan pinta-ala on huomattavasti suurempi kuin kenkien. Lumikengillä kävelijän paine hangen pintaan on pienempi kuin pelkillä kengillä. Tämän seurauksena hanki kantaa lumikenkäilijää paremmin.
). Mitä pienempi pinta, sitä suurempi paine. Esimerkiksi lumikenkien pohjan pinta-ala on huomattavasti suurempi kuin kenkien. Lumikengillä kävelijän paine hangen pintaan on pienempi kuin pelkillä kengillä. Tämän seurauksena hanki kantaa lumikenkäilijää paremmin.
Vaikka lumi onkin lähellä jäätä, niin palataan siihen jäähän. Henkilön paino siis kohdistuu kengänpohjan kokoiseen pinta-alaan.
Niin. Keskiarvo aikuisen ihmisen jalan pituudelle on  ja leveydelle
ja leveydelle  (kuva 1).
(kuva 1).

Kuva 1: Keskimääräisen aikuisen kengän koko.
Laskemisen helpottamiseksi mallinnetaan kengän pohjaa suorakulmiona. Kengänpohjan pinta ala on siis  . Jään pintaan kohdistuva paine on
. Jään pintaan kohdistuva paine on
Eli aiheutamme astuessamme jään pinnalle pintaan paineen, jonka suuruus on parikymmentä kPa.
Ja itse asiassa kengän pohjan aiheuttaman paineen lisäksi mukana on kaikissa tilanteissa myös normaali ilmanpaine, noin 100 kPa. Eli kengän aiheuttama paine on vaatimaton jo pelkkään ilmanpaineeseen verrattuna.
Onko tämä paine riittävän suuri sulattamaan jään pinnan vedeksi?
Tuohon vastataksemme meidän on tarkasteltava veden faasikaaviota.
Eli sitä kaaviota, jossa on aineen olomuotoja eli tilanteissa?
Joo, faasi on toinen sana olomuodolle. Faasikaaviolla yleensä kuvataan aineen olomuotoja eri lämpötiloissa ja paineissa. Videossa 1 käydään läpi faasikaavion tulkintaa.
Video 1: Faasimuutokset ja faasikaaviot.
Jos jään lämpötila on  , niin normaalissa ilmanpaineessa eli
, niin normaalissa ilmanpaineessa eli  (1 atm = 1 atmospheric pressure) veden olomuoto on jää, eli kiinteä (Kuva 2, sininen alue). Faasikaavioon (Kuva 2) on merkitty punaisella ympyrällä jään olomuoto olosuhteissa
(1 atm = 1 atmospheric pressure) veden olomuoto on jää, eli kiinteä (Kuva 2, sininen alue). Faasikaavioon (Kuva 2) on merkitty punaisella ympyrällä jään olomuoto olosuhteissa  ja
ja  .
.
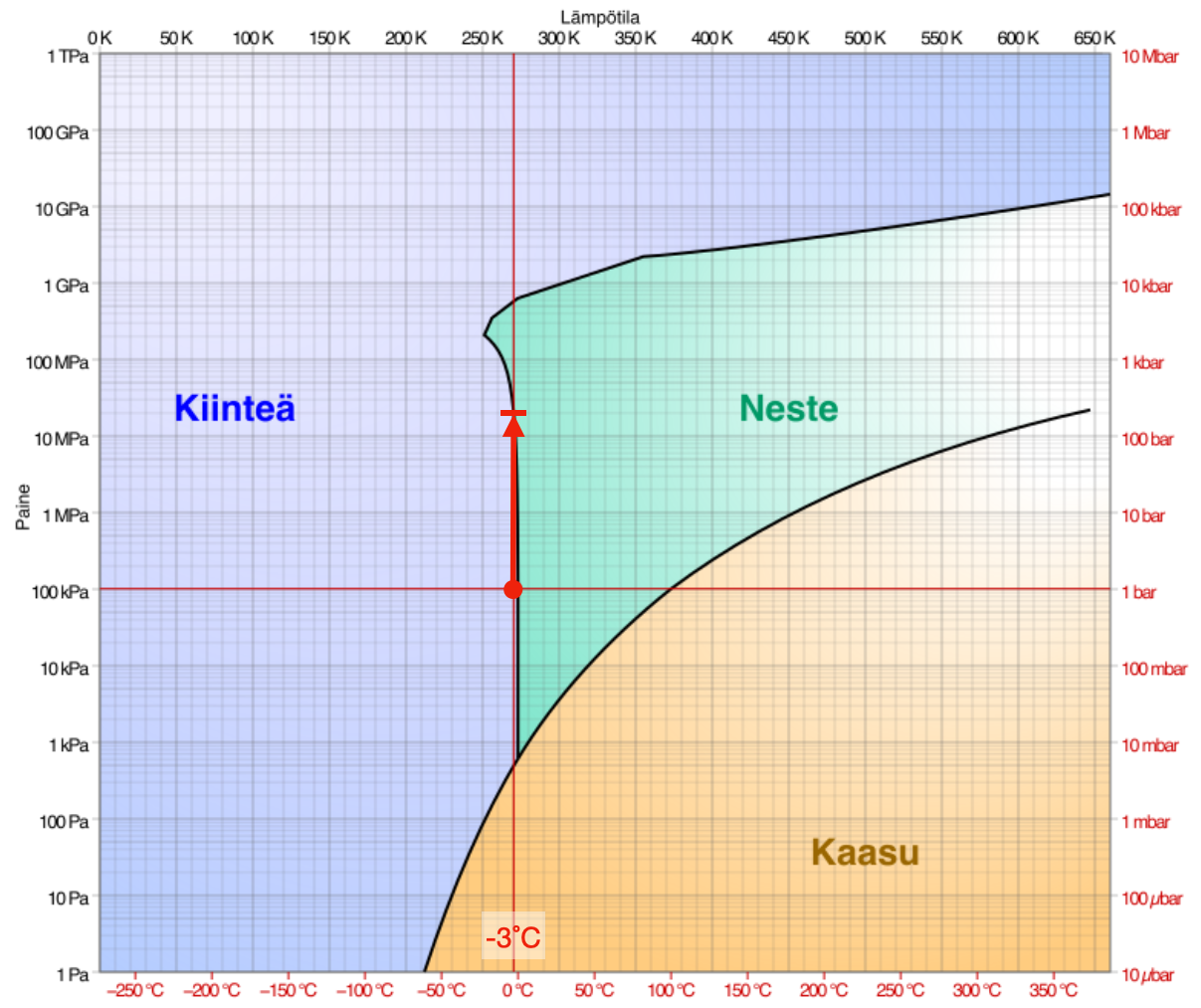
Kuva 2: Veden faasikaavio. Lämpötila on lineaarisella ja paine logaritmisella asteikolla. Punainen ympyrä esittää vettä 270 K lämpötilassa ( ) ja normaalissa ilmanpaineessa; olomuoto on kiinteä (jää). Nuoli osoittaa kuinka tässä lämpötilassa jään sulattamiseen tarvittaisiin noin
) ja normaalissa ilmanpaineessa; olomuoto on kiinteä (jää). Nuoli osoittaa kuinka tässä lämpötilassa jään sulattamiseen tarvittaisiin noin  :n paine.
:n paine.
Faasikaavioon veden nestemäinen olomuoto on merkitty vihreällä värillä. Näemme kaaviosta, että veden sulattaminen edellyttäisi joko lämpötilan tai paineen nousua. Kaavioon on merkitty sulattamiseen tarvittava paine, kun lämpötila ei muutu: tarvittava paine olisi jopa  . Kengän pohjan alla oleva paine
. Kengän pohjan alla oleva paine
on vain noin 0,6 prosenttia olomuodon muutokseen tarvittavasta paineesta.
No mutta siis periaatteessa olisi mahdollista sulattaa jäätä sopivan painon alla?
Kyllä, ainakin tuossa  :n lämpötilassa. Voidaan laskea, että mikä pitäisi olla henkilön massa, jotta jää sulaisi jalan alla. Jätetään tämä itsenäiseksi laskuksi, mutta vastauksena henkilön massan tulisi olla n.
:n lämpötilassa. Voidaan laskea, että mikä pitäisi olla henkilön massa, jotta jää sulaisi jalan alla. Jätetään tämä itsenäiseksi laskuksi, mutta vastauksena henkilön massan tulisi olla n.  . Toisaalta voidaan laskea, että miten pieni pinta-ala tarvittaisiin, jotta
. Toisaalta voidaan laskea, että miten pieni pinta-ala tarvittaisiin, jotta  kg painoinen henkilö sulattaisi jään allaan. Jätetään tämänkin itsenäiseksi laskuksi, mutta vastaus on noin
kg painoinen henkilö sulattaisi jään allaan. Jätetään tämänkin itsenäiseksi laskuksi, mutta vastaus on noin  eli huomattavan vähän.
eli huomattavan vähän.
Mutta entä kenkien kuviot? Ei koko kengän pohja välttämättä kosketa jäätä. Tai vaikka kapeakantaiset korkokengät?
Erittäin hyviä huomioita. Jään sulamisen kannalta keskeistä onkin juuri se mikroskooppinen pinta-ala, joka paineen aiheuttaa. Usein nämä alat ovat murto-osia silmillä nähtävästä, makroskooppisesta pinta-alasta. Todelliset paineet pienemmällä pituusskaalalla tarkasteltuna tosiaan ovat suuremmat, mutta nekään eivät ole riittävän suuria sulattamisen. Kaaviosta 2 voi nähdä, että lämpötilan laskiessa tarvittavan paineen määrä kasvaa ja noin alle 25 asteen pakkasessa jäätä ei saa enää sulatettua missään paineessa.
Mutta kovalla pakkasella jää ei olekaan niin liukasta kuin suvikelillä.
Paukkupakkasissa jään nihkeämpi tuntu johtuu ensisijaisesti jään pinnan rakenteen karhentumisesta (kosteuden härmistyminen jään pintaan kitkaa kasvattaviksi jääkiteiksi).
Okei eli syynä ei siis ole paine. Mutta mitenkäs sitten muut vaihtoehdot?
Mietitääpä sitten vaihtoehtoa B. Kävellessämme jäällä, kenkien ja jään välinen mikroskooppinen suhteellinen liike synnyttää kitkaa, joka lämmittää jään pintaa. Luistellessa liikekitkan syntyminen lienee kaikkein ilmeisintä. Onkin totta, että kitkan vaikutuksesta syntyy lämpöä. Sen voi kokea itsekin hieromalla käsiä yhteen. Tämä lämpö aiheutuu kahden pinnan välisten hetkellisten kemiallisten sidosten muodostumisesta ja murtumisesta.
Eli kitka-selityksessä ollaan oikeilla jäljillä?
Ehkäpä, vaikka veden tiedetään olevan huonompi liukaste kuin vaikka ruokaöljyn. Mutta jätetään ajatus kitkasta taka-alalle ja siirrytään miettimään vaihtoehtoa C, eli jään pinnalla olevaa, vapaista molekyyleistä johtuvaa liukastekerrosta.
Vesi on siitä mielenkiintoinen aine, että sen kiinteä olomuoto on nestemäistä harvempaa. Lähes kaikilla muilla aineilla kiinteä olomuoto on nestemäistä tiheämpää. Tämä poikkeava ominaisuus johtuu vetysidoksista. Muistatkin varmaan, että vesimolekyylit (eli  ) koostuvat kahdesta vetyatomista (
) koostuvat kahdesta vetyatomista ( ) ja yhdestä happiatomista (
) ja yhdestä happiatomista ( ) (Kuva 3).
) (Kuva 3).
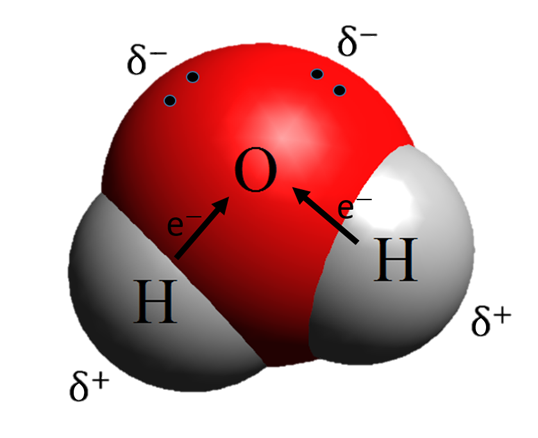
Kuva 3: Vesimolekyyli
Vetyatomien ja happiatomin välillä on kovalenttiset sidokset. Ne siis jakavat elektroninsa. Jakautuminen ei kuitenkaan ole tasainen, vaan happiatomilla on negatiivinen ja vetyatomeilla positiivinen osittaisvaraus. Atomien osittaisten varausten ja geometriansa vuoksi vesimolekyyli on polaarinen. Vesimolekyylin negatiiviset happiatomit siis vetävät puoleensa toisen vesimolekyylin negatiivisia vetyatomeita. Tästä polaarisuudesta ja vetyatomien käyttäytymisen kvanttimekaanisesta luonteesta aiheutuu veden ainutlaatuinen tapa sitoutua vetysidoksin.
Nestemäisessä vedessä vesimolekyylien liikkuessa toistensa lomitse vetysidokset rikkoutuvat ja syntyvät uudelleen jatkuvasti. Veden lämpötilan laskiessa kohti jäätymispistettä molekyylien nopeus vähenee ja ne alkavat liikkumaan tahmeammin. Veden jäätyessä molekyylit muodostavat kiinteän rakenteen, jossa suurin osa vesimolekyyleistä on yhteydessä useampaan toiseen vesimolekyyliin vetysidosketjuilla (kuva 4).
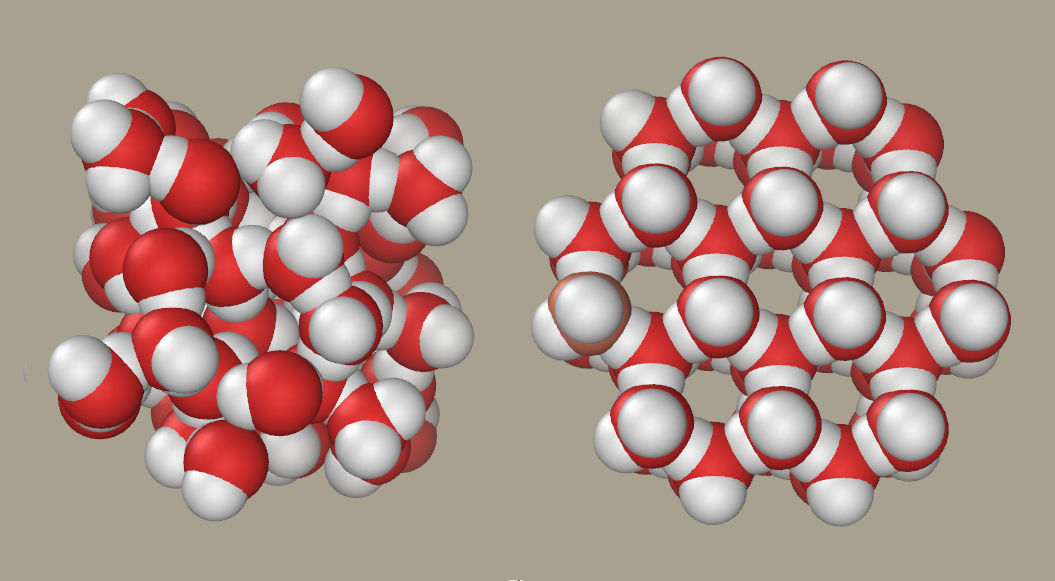
Kuva 4: Vasemmalla vesi on nestemäisessä olomuodossa ja vesimolekyylit liikkuvat toistensa lomitse. Oikealla vesi on kiinteässä olomuodossa ja vesimolekyylit muodostavat kiinteän rakenteen.
Miksi sanoit, että “suurin osa”?
Oletpa tarkka! Vesimolekyylit kiinteän jään pinnalla ovat sitoutuneet rakenteeseen heikommin kuin jään sisässä. Pinnalla molekyyleillä kun on vähemmän sidoksia toisten vesimolekyylien kanssa. Tämä näkyy kuvassa 4 oikealla: vertaa kiinteän muodon pinnalla olevia molekyylejä sen keskellä oleviin. Ylimmän kerroksen molekyylit siis irtoavat toisista vesimolekyyleistä herkemmin lämmön vaikutuksesta. Tämä luo jään pintaan kerroksen vapaita vesimolekyylejä eli nestemäistä vettä, mikä aiheuttaa liukkautta.
Mutta juurihan sanoit, ettei nestemäinen vesi ole kovin hyvä liukaste.
Näin on ja nyt alammekin lähestyä tämän vastauksen pihviä.
Kun kävelet jäällä, kenkiesi ja jään välisen kitkan ansiosta jään pinnalta sulaa erittäin ohut kerros jäätä nestemäiseksi vedeksi. Tämän kerroksen paksuus on vain sadasosa hiuksen paksuudesta, eli mikrometrin murto-osia. Olisi helppo olettaa, että kaikki nestemäinen vesi käyttäytyy samalla tavalla, mutta näin ei ole. Tämä hyvin ohut kerros vettä käyttäytyy eri tavalla kuin paksumpi kerros vettä. Ohuen kerroksen viskositeetti (nesteen “tahmaisuus”) voi olla jopa 100 kertaa paksua vesikerrosta suurempaa, mikä ei ole kaukana ruokaöljyn viskositeetista. Ohuella kerroksella vettä on ikään kuin yhtä aikaa nesteen ja kiinteän aineen ominaisuuksia. Se ei palaudu takaisin muotoonsa puristuksen alla kuten kiinteä aine. Tämä ns. rajapintavesi saa aikaan huomattavasti pienemmän kitkan ja liukkaamman pinnan kuin paksumpi vesikerros.
Ahaa...
Jep, liukkauden selittäminen oli yllättävän monitahoista. Ei ihmekään että sen selvittämisessä kesti aikaa. Koulussa opittu selvä jako eri olomuotojen välillä ei aina pidäkään paikkaansa. Fysiikassa ja kaikessa tieteessä pitää aina muistaa, että tietomme oikeellisuudesta ei ole ikinä täyttä varmuutta. Uusien tutkimustulosten valossa ymmärryksemme maailmasta tarkentuu. Joskus vanha tieto tarkentuu tai se voidaan jopa hylätä kokonaan. Tämä jään liukkaus on hyvä esimerkki siitä, että näinkin arkisesta ilmiöstä on saatu lisätietoa vasta viime vuosina. Alankomaalaiset tutkijat julkaisivat tämän selityksen taustalla olevat tulokset vasta vuonna 2021. Ymmärrettävästi on todella vaikeaa tutkia ohuita vesikerroksia, joten nämäkin tulokset ovat mahdollistuneet mittauslaitteiden ja -tekniikan kehityksen myötä.
Onko jotain muita arkisen oloisia ilmiöitä, joiden taustalla olevaa fysiikkaa ei vielä tunneta?
Onhan niitä. Esimerkiksi hankaussähkö on hyvin arkinen ilmiö jonka huomaa hiusten kohoamisena pystyyn kun niitä hangataan ilmapallolla tai sähköiskuina ovenkahvoista huoneissa, joissa on kokolattiamatto. Tutkijoilla ei silti ole vielä kunnollista selitystä sille, että miksi jotkut kappaleet varautuvat negatiivisesti ja toiset positiivisesti näissä tilanteissa. Jos hankaussähköä ymmärrettäisiin paremmin, voitaisiin suunnitella parempia suojauksia huoltoasemille ja muihin paikkoihin joissa kipinän syntyminen on epätoivottua.
| Tiviistelmä |
| Jään liukkauden syy on ollut mysteeri viime vuosiin saakka. |
| Tutkimuksissa on selvennyt, että jään pinnasta sulaa kitkan vaikutuksesta äärimmäisen ohut vesikerros, jolla on sekä nestemäisen että kiinteän veden ominaisuuksia. |
| Tämä ohut kerros aiheuttaa jään liukkauden. |
| Hankaussähkön syntymekanismi ja monet muut arkiset ilmiöt ovat vielä ilman tyydyttävää fysikaalista selitystä. |



